物理化学
化学
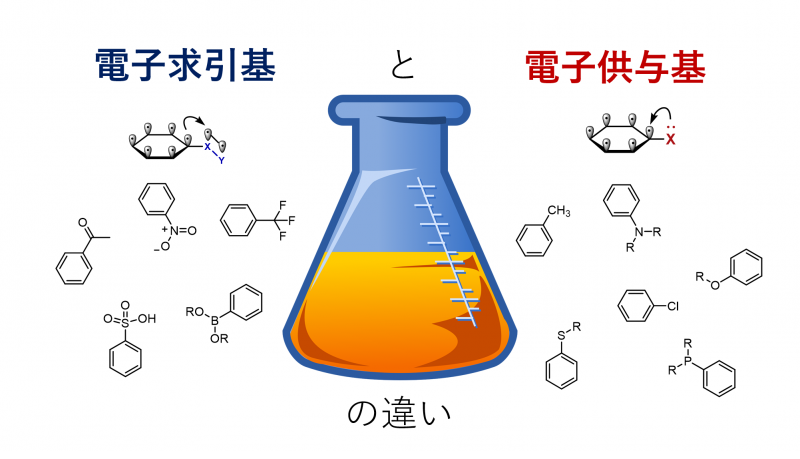
(日本語) 【電子求引基・電子供与基】の違いを理解する。芳香族求電子置換反応でのオルト/パラ配向性、メタ配向性など
Sorry, this entry is only available in 日本語.

chelate
キレート(chelate)という金属と有機化合物間で生じる相互作用は、薬の飲み合わせなどでよく問題になります。結構な頻度で起こる事なので、科学的な理解が必要であり、国試でも狙われ易いです。 ポイント sp2 キレートとは? 簡単にいえば、ミネラルみたいな金属にS, N, Oのような原子が張りついてしまうというものです。 S, N, Oの特徴としては非共有電子対(ローンペア)を持っているということですね。 金属原子にある電子を受け入れるスペース(空軌道)にこれらの原子がローンペアを与えることで、くっついてしまうためです。 医薬品が金属とくっついてしまうと何が悪いかというと。 薬に使われる金属は「Fe2+」「Mg2+」といった、イオンなんです。身近なイオンといえば、食塩「NaCl」がありますね。 ご存知のように、ミネラルは水に溶けますよね?ミネラルウォーターとかあるように。 一方、医薬品は脂溶性でなければ、血液中に入れないんですよね。 ここで、 ミネラルを「M+」、含窒素医薬品を「N-Med」とします。 医薬品中のNと金属イオンM+がくっつくと「+M-N-Med」になります。 つまり医薬品がイオンになったようになるんです。となると、医薬品が水溶性になってしまいます。 こうなると、血液中に入ることができなくなります。 これがいわゆる ニューキノロン系抗菌薬やテトラサイクリンとカマグ などの相互作用ですね。 体の中にも鉄ってありますよね、血液はもちろん、CYP450など。 一酸化炭素は血中鉄とキレートして、酸素の運搬を止めます。 アゾール系の薬はCYPの鉄とキレートし、酸素を使った代謝を止めます。 ここから、一気に化学的な内容になります。 すべてのローンペアが金属に配位してたら、人はすでに死んでます。 キレートしやすい条件があります。 ・空のp軌道を持った複素原子(S, O, N) C=N、CN、COなど ・多座配位(一分子の中に多くの配位性ローンペア) 理由はバックドネーション 例えば、シメチジンの構造を見てみると…
生化学
How to treatment hay fever
I’d like to Check Point!! ・aaa ・ Science Point!! ・aaa ・ explanations
envelope
ウイルスを構造的特徴で分類すると、大きく2種類あります。エンベロープがあるか、ないかということです。 エンベロープの正体は脂質二重膜であり、人間がもつ細胞膜と同じです。 エンベロープを持つか、もしくは持たないかの違いで、感染の様式や除菌方法が大きく変わります。 先にポイントですが、 Point‼ ・エンベロープなしは、消化器や内臓に感染 エタノール消毒が効きにくく、塩素系以上の強さの消毒が必要。 ・エンベロープありは、肺や気管支などの呼吸器に感染 エタノール消毒も結構有効であり、塩素消毒も有効。 いい文献があるので先に紹介しますね。 ウイルスの構造上の特徴と消毒感受性について2008, No 59 以下エンベロープの有り無しで分類していきます。 消化管に感染するウイルスはエンベロープ(-) エンベロープを持つウイルスは胃酸で死んでしまいます。つまり、消化管感染するウイルスは 経口感染するウィルスにはエンベロープがありません。たとえば、C型肝炎ですが、専ら注射感染が問題になります。ただし、経口感染って聞いたことありますか?実際に、C肝ウィルスは、エンベロープをもっています。 上気道感染ウイルスは、エンベロープ(+) 受容体を介して感染するため 科学的ポイント エンベロープは二重膜ですが、どう壊れるのでしょうか? エタノールの作用とすれば、界面活性作用が最もでしょう。 アルデヒド系統はタンパク変性? イオン系は… 参考文献 ヤクハンQ&A


