「メイロン注(炭酸水素ナトリウム注)を生食に希釈してはいけない理由は??」
という、1件の相談があったので、調べてみました。
この質問を受けたとき、薬局薬剤師である私は、普段注射剤は取り扱っていないこともあり、質問に即答できませんでした。
ですが、何も推測を立てないのはいかがなものかと思い、混合できない理由について推測は立ててみました。
「pHの変化で炭酸が遊離するのか??」と。
確かにメイロンは、炭酸水素ナトリウムが主成分であるがゆえにpH変化に弱い、という特徴を有しています。
では実際どうなのでしょうか?調べた結果を以下にお示しします。
メイロン注の使用目的
メイロン注の使用目的は、メニエール症候群のような、内耳系疾患の改善やアシドーシスの是正だったりします。
適応は奥が深そうだったので、そのうち別記事で紹介します。
臨床現場で非常によく使用される、メイロン注ですが…
その成分は炭酸水素ナトリウムであり、配合によってはpHが変化し、炭酸ガスが発生するため、いろいろな不都合が生じてしまう薬剤です。
NaHCO3 → H2CO3 → H2O + CO2↑
化学反応式で示せば、このような感じになり、CO2が遊離してしまいます。
つまり、様々な溶液と配合変化を起こしやすく、極めて注意が必要な注射剤になります!
メイロンの使用方法(希釈、投与など)
メイロンの適切な希釈溶液
いい文献があったので紹介します。
輸液に炭酸水素ナトリウム注射液(メイロン®静注)を混合する時の留意点
大塚製薬さんが出している記事です。
その中からデータを引用します。以下のデータは、メイロンと各輸液類を混合した場合の最終pHを示したものです。最終pHが小さいものほど、炭酸が遊離して、体積変化による液面の低下が引き起こされます。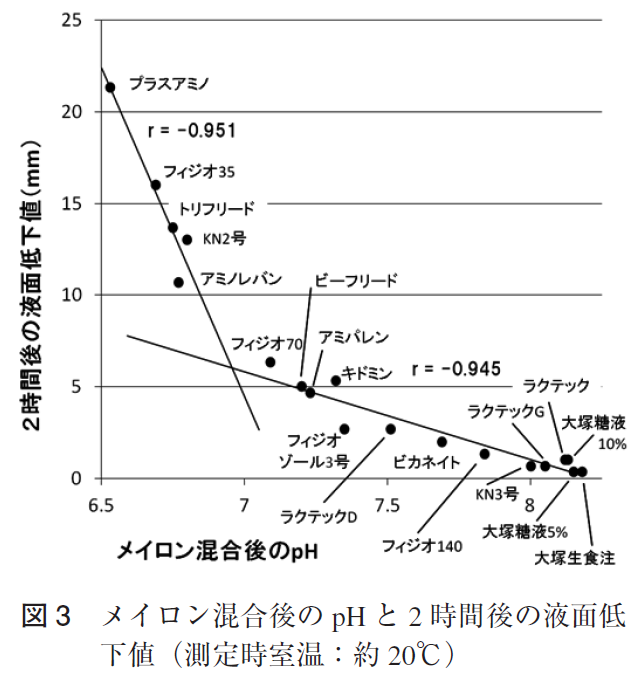
配合変化としては、生食、糖液など大抵のものは大丈夫との結果が得られています。
一方、KN3号やフィジオに溶解すると、以下の写真のようになってしまうみたいです。
ガスが発生することで内圧が上がり下の写真(図4)のような変化が生じてしまいます。
液面が下がる=ガスが発生しているということです。
輸液に炭酸水素ナトリウム注射液(メイロン®静注)を混合する時の留意点より引用
図3のデータを見てみると、生食とメイロンの混合で、配合変化(ガスの発生)が生じるということはほとんどなさそうです。
生食が好ましくない理由は??
ここで初めに紹介した、質問に対する仮説
「pHの変化で炭酸が遊離するのか??」
ですが…上記のデータを見てもわかるように、
メイロン(炭酸水素ナトリウム)は、配合後のpHが7.5程度までであれば、ほとんどガスは遊離しないようです。
pH=7でも大してガスは出ない結果となっていますね。
つまり…生食(pH=7)と、メイロン(pH=7.9)を混ぜたところで、ガスはほとんど出ない!
(生食とメイロンを混ぜても、メイロンがもともと塩基性製剤なので、炭酸水素イオンのpKaを大きく下回るpHに至らない。詳しくは、本記事の下を読んでください。)
ということになります。
私の仮説「ガスが出てしまう」は見事に外れてしまいました。
ではなぜ生食はダメなのでしょうか???
いろいろ調べたところ、NaのmEqに注意する必要がありそうです。
Naのmeqを抑えるため?
人に必要な一日のNa量は、3~4mEq/kg/Day程度です。ざっくり50㎏の人で150mEq/dayです。
メイロンは
7%製剤が833mEq/1000ml
8.4%製剤が、1000mEq/1000ml
生食は
154mEq/1000ml
8.4%メイロン 20 mL 1本を生食250 mLに溶かした場合、20+38.5=58.5 mEqとなります。
150までだから大丈夫じゃん!と思うかもしれませんが、食事から摂る分もあります。
なので、HPの観点から、配合変化的には問題ないようですが、ナトリウム量からは推奨されないようですね。
目的によっては希釈をして投与しない方がいいのでは??
という意見もみつかりました。これは、「血液のpH是正のために投与するのに、薄めて(pHを下げて)どうする!」ということです。
確かに、希釈して塩基としての濃度を下げてしまうと、pH是正力は低下してしまいます。その観点から言えば、無駄な希釈は回避すべきだと思いますね。
Science Point!!メイロンの配合変化を科学的に分析してみましょう!!
pHは7.5までにセーブ
中性の輸液であれば、炭酸ガスの発生は問題なし!
図3のグラフを見ていただくと、pH7.5から炭酸の遊離が始まるようですね。
それもそうです。炭酸(H2CO3)が炭酸イオン(HCO3-)になるpKaは約6.4。
メイロン注のpHが6.4になった時、H2CO3とHCO3-は1:1になります。
H2CO3は、二酸化炭素(CO2)が水に溶けてできたものです。
CO2は比較的水に溶けやすい気体ですが、ほとんどが水に溶け込まずガスのまま存在しています。
つまり、メイロン注のpHが6.4になった時、約半分のCO2が発生してしまいます。
pHが7.5であれば、H2CO3とHCO3-は1:10程度であるため、CO2の発生量はほとんどないと考えられます。
生食とメイロンを混ぜても、メイロンがもともと塩基性製剤なので、
中性のメイロンをいくら混ぜても、pHは7にしか近づきません。
つまり、これではCO2ガスは発生しないのも当然です。
メイロンを混ぜるときには、相手側のpHをしっかり確認して下さいね。
最後まで読んでいただきありがとうございました。
