キレート(chelate)とは
キレートは複数の配位座を持つ配位子(多座配位子)が金属と錯体を形成することを言います。
言えば、一つの分子に配位結合が集合したもので、エントロピーの増大(自由度の増大)が、キレート錯体形成の駆動力となります。詳細には、一つの分子がより多くの配位座を持つ場合に強く形成されやすくなります。
EDTAは有名で、配位点を多く持ち金属を補足します。採血管でカルシウムによる血栓形成を阻害するために用いられたりします。
医薬品の中には偶然キレートの形成能を持ってしまったものもあります。キレート形成能の有無は、薬の飲み合わせなどでよく問題になります。結構な頻度で起こる事なので、科学的な理解が必要であり、国試でも狙われ易いです。
薬剤師、薬学生の方は以下の2点をよく理解しておきましょう。
Check Point!!
・二重結合や三重結合をもった窒素(sp2 or sp 混成)がキレートしやすい!!
キレートと医薬品
キレートや配位を簡単にいえば、ミネラルみたいな金属にS, N, Oのような原子が張りついてしまうというものです。そもそも、医薬品が「Fe2+」「Mg2+」といった金属とキレートを形成すると何が悪いかというと、低極性の有機分子がイオンと結合するために溶解度などの物性が大きく変化してしまいます。
身近な例を挙げれば、カルシウムイオン「Ca2+」がありますね。言うまでもなくミネラルウォーターとかに含まれています。つまりミネラルは水に溶けています。つまりイオンは極めて水溶性が高いのです、ここで、ミネラルを「M+」、含窒素医薬品を「N-Med」とします。医薬品中のNと金属イオンM+がキレートを形成すると「+M…N-Med」になります。こうなると、医薬品が水溶性になってしまい、細胞膜を通過して血液中に入ることができなくなります。これがいわゆるニューキノロン系抗菌薬やテトラサイクリンとカマグなどの相互作用ですね。
メモ
錯体はよく色を持ちますが、これはキレートを形成した時に生じる新たなd軌道バンドギャップが小さいために、呈色します。
強力なキレート形成(配位形成)と化学構造
ここには、学生時代に友人に話して「ありがとう」と言ってもらえた話を載せます。
キレート能の有無を判断するために構造で着目すべきなのは、以下の二点です
・強力な配位官能基の有無
・配位結合を形成しうる官能基の数
強力な配位官能基は、一つだけでも金属との相互作用を示します。
配位しやすい原子
配位は非共有電子対(ローンペア)が接着剤になるので、これを持つS, N, O, Pなどの原子が配位能力を持ちます。
言うまでもありませんが、医薬品構造中に多く含有される原子は、窒素です。しかし、すべての窒素が金属に強く配位するわけではないのです。(この辺が化学に慣れていない人がキレートを深く理解できない原因だと思います。)もしすべての窒素原子が金属に強く配位したら、ほとんどの全ての薬がCYPを阻害したり、消化管から吸収されないといった問題が生じ、まず医薬品として成り立ちません。
ローンペア+p軌道を一つの原子上に持つこと
ローンペアとp軌道が一つの原子上に存在していると、より強力に配位します。これをわかりやすいように段階的に説明します。先に下の図を見てください。
強い配位は、
1. 金属カチオンへのローンペア電子供与
2. 金属電子の逆供与
で形成されます。
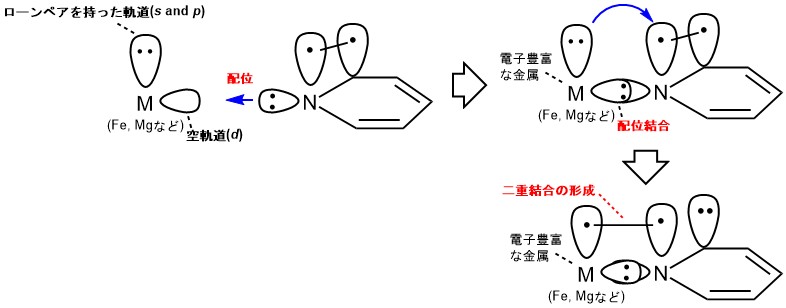
1.金属イオンにローンペア電子を供与(単結合の形成)
そもそも配位とは、N, S, O, Pなどのローンペア(-)が金属イオン(+)と結合を形成するものです。「金属イオンは電子を失った状態なので、電子欠損」であり配位子のローンペアを受容できると考えてください。配位子の電子を受容することで単結合が形成されます。
一応、深いことも言っておきます(興味ある人だけ)
例えばFe2+の3d軌道は、3つの電子対(6e)と2つの空軌道から構成されています。さらに、2+イオンですので最外核の4sは、中性原子状態で持っていた2電子を失い、空軌道となっています。この4s空軌道やまだ空いている内側のd軌道に、配位子のローンペアが電子が収容されます。3d軌道が先に電子を収容するか、4s
2. 金属電子の逆供与(二重結合の形成)
ローンペアが配位したあと、金属は電子を十分に獲得した状態となります。この時、もし窒素上に電子欠損なp軌道が存在していた場合、逆供与(バックドネーション)が発生し、金属-配位子結合はπ結合(d-p結合)を形成することがあります。これで、二重結合が作られ、とても強く金属と結合します。
強力に結合する配位子の例
特に金属に強く配位しやすいものは、sp2やsp混成を持つ窒素です。
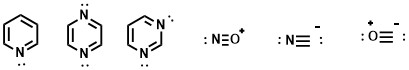
上記の化学種はsp2軌道にローンペアを持っており、さらに電子欠損なP軌道を持っています。皆さんも覚えのある構造ではないでしょうか?(すいませんトリアゾールとか入れ忘れました…)
特に三重結合(sp混成)を持つ化学種には超要注意です!
図右側の三重結合をもった、シアンや一酸化炭素は、血中のヘム鉄に配位して、酸素欠乏を引き起こし、死に至らしめてしまう危険なガスですよね。また、冒頭でも触れたEDTAなどの多座配位(一分子の中に多くの配位性ローンペア)は、エントロピー的に有利なためキレートを作りやすいので注意が必要です。
キレート能を有する代表的な医薬品
代表的な医薬品を見てみましょう…思いましたが、すみません、編集中です。
一番言いたい部分は既に述べたので、この辺は後々編集します。
いかがでしたでしょうか?添付文書の構造式を見てみたくなってきませんか??
最後まで読んでいただきありがとうございました。
